國家組織人工關節集中帶量采購周期即將期滿,為鞏固高值醫用耗材集中帶量采購改革成果,根據國務院辦公廳《關于印發治理高值醫用耗材改革方案的通知》(國辦發〔2019〕37號)、國家醫保局等八部門《關于開展國家組織高值醫用耗材集中帶量采購和使用的指導意見》(醫保發〔2021〕31號)要求,著眼于穩定價格水平、穩定臨床使用、穩定生產供應,引導行業和社會形成長期穩定預期。按照國家組織、聯盟采購、平臺操作的總體思路,全國各省份組成采購聯盟,委派代表組成國家組織高值醫用耗材聯合采購辦公室(以下簡稱“聯合采購辦公室”),代表各地區公立醫療機構(含軍隊醫療機構,下同)及自愿參加的社會辦醫療機構等開展國家組織人工關節集中帶量采購協議期滿接續采購,由天津市醫藥采購中心承擔日常工作并負責具體實施。現就有關事項公告如下:
一、采購產品
本次集中帶量采購產品為初次置換人工全髖關節(以下簡稱髖關節)、初次置換人工全膝關節(以下簡稱膝關節),含增材制造技術(即3D打印)類產品。定制化增材制造技術產品可自愿參加。
1.髖關節。髖關節以股骨柄、股骨頭、髖臼內襯、髖臼杯各1件,髖臼螺釘2枚組成產品系統。股骨柄和髖臼杯材質包括鉻合金(含鈷鉻鉬合金、鈷鉻合金)、鈦合金(含純鈦)、鉭金屬。股骨柄和髖臼杯假體在體內的固定方式包括生物學涂層固定和骨水泥固定兩種。髖關節產品系統根據股骨頭和髖臼內襯材質組合,分為以下三個產品系統類別開展集中帶量采購。
(1)陶瓷-陶瓷類髖關節產品系統,要求股骨頭和髖臼內襯材質均為氧化鋯增韌高純氧化鋁基復合材料。
(2)陶瓷-聚乙烯類髖關節產品系統,要求股骨頭材質為氧化鋯增韌高純氧化鋁基復合材料;髖臼內襯材質為聚乙烯,包括高交聯聚乙烯、高交聯聚乙烯(含抗氧化劑)、超高分子量聚乙烯。
(3)合金-聚乙烯類髖關節產品系統,要求股骨頭材質包括鈷鉻鉬合金、鋯鈮合金(表面經氧化處理的鋯鈮合金產品可自愿參加);髖臼內襯材質為聚乙烯,包括高交聯聚乙烯、高交聯聚乙烯(含抗氧化劑)、超高分子量聚乙烯。
2.膝關節。膝關節以股骨髁、脛骨墊片、脛骨平臺、髕骨假體各1件組成產品系統。股骨髁和脛骨平臺材質包括鉻合金(含鈷鉻鉬合金、鈷鉻合金)、鈦合金(含純鈦)、鋯鈮合金、鉭金屬;脛骨墊片材質為聚乙烯,包括高交聯聚乙烯、高交聯聚乙烯(含抗氧化劑)、超高分子量聚乙烯。膝關節作為一個產品系統類別開展集中帶量采購。
二、企業資質
申報企業為已取得本次集中帶量采購產品合法資質的醫療器械注冊人(含備案人,下同),滿足以下要求的,均可參加。其中,境外醫療器械注冊人應當指定我國境內企業法人協助其履行相應的法律義務,委托其作為申報企業。符合采購產品和企業資質要求的企業須于規定時間內在國家醫保服務平臺-國家組織高值醫用耗材集中采購信息填報系統維護產品信息。
(一)申報產品應當符合國家有關部門的質量標準要求,并按國家有關部門要求組織生產。
(二)申報企業須明確供應區域,并承諾申報的各產品對應所有規格型號在采購周期內滿足該區域采購需求。
(三)申報企業和醫療器械注冊人應遵守《中華人民共和國專利法》《中華人民共和國反不正當競爭法》等相關法律法規。
(四)申報企業和醫療器械注冊人未被列入當前《全國醫藥價格和招采失信企業風險警示名單》,未被聯合采購辦公室列入當前“違規名單”。
(五)同一醫療器械注冊人的產品不得委托不同企業申報。
(六)不同醫療器械注冊人委托同一家企業申報的,各委托企業之間及委托企業和受托企業之間均視為存在關聯關系;不同醫療器械注冊人委托不同企業申報,但受托企業為同一實際控制人或存在控股關系的,各委托企業之間、各受托企業之間及委托企業和受托企業之間均視為存在關聯關系;不同醫療器械注冊人間,如為同一實際控制人或存在控股關系的,視為企業間存在關聯關系;不同醫療器械注冊人委托不同企業申報,但委托企業為同一實際控制人或存在控股關系的,各委托企業之間、各受托企業之間及委托企業和受托企業之間均視為存在關聯關系。
(七)醫療器械注冊人為同一實際控制人或存在控股關系的,如委托同一家企業申報,視為同一申報企業,應提交一份唯一報價的申報材料;醫療器械注冊人非同一實際控制人,且不存在控股關系的,如委托同一家企業申報,視為不同申報企業,應分別提交申報材料。
三、醫療機構范圍
聯盟地區有使用人工關節的公立醫療機構(含軍隊醫療機構,下同)均應參加。醫保定點社會辦醫療機構在承諾遵守本次集采規定的前提下,按所在省(區、市)的相關規定參加。
四、采購規則
(一)意向采購量
聯合采購辦公室組織企業自主申報組成產品系統,組織醫療機構填報采購需求量,并匯總采購需求量后按一定比例形成意向采購量。
1.企業按要求自主申報組成產品系統。企業按照本公告“一、采購產品”中的要求,維護屬于本次集采范圍的全部醫療器械注冊證產品信息并組成產品系統,確保滿足臨床使用需求,確認供應區域范圍,并填報供應中國市場的年最大產能信息。
2.醫療機構填報采購需求量。醫療機構結合臨床歷史使用狀況、醫療技術進步等因素,從有意愿供應本轄區的企業中選擇產品系統,并如實準確填報每個產品系統未來一年的需求量。
3.聯合采購辦公室匯總醫療機構填報的采購需求量,按一定比例明確本次集中帶量采購的意向采購量。
(二)競價單元
為確保臨床使用和供應穩定,綜合考慮醫療機構需求、企業供應意愿和供應能力等因素,將企業分單元分別競價。同一產品系統類別下,同時滿足如下條件的申報企業進入A競價單元,其他進入B競價單元:
1.根據醫療機構需求量由多到少依次排序,取該產品系統類別累計需求量前85%(含)且能供應全國所有地區的企業;
2.企業申報的陶瓷-聚乙烯類髖關節產品系統、合金-聚乙烯類髖關節產品系統的髖臼內襯至少有一個產品系統具備高交聯聚乙烯或高交聯聚乙烯(含抗氧化劑)材質。
如進入A競價單元企業數量不足7家,在能供應全國所有地區且滿足上述條件2且需求量大于0的有效申報企業中,根據醫療機構需求量由多到少依序遞補至7家。如能供應全國所有地區且滿足上述條件2且需求量大于0的有效申報企業不足7家,則全部進入A競價單元。當擬遞補的企業需求量為0時不予遞補。
(三)競價規則
企業以產品系統類別申報價格,每一個產品系統類別的所有產品系統僅允許有一個申報價。滅菌與非滅菌不作區分。
申報價格包含產品系統內各部件價格、配送和配套使用工具及伴隨服務費用,企業報價時需標明產品系統中每個部件的單價,伴隨服務不單獨報價(具體比價方法另行公告)。同一部件產品在髖關節或膝關節不同產品系統類別和產品系統中價格應保持一致;同一部件產品不同規格型號價格應相同,同一企業同一部件(髖臼螺釘、髕骨假體除外)的不同產品保持合理價差;同一申報企業髖臼螺釘價格應保持一致;同一申報企業髕骨假體價格應保持一致。
當申報企業產品系統類別的申報價格與產品系統內各部件價格之和不同時,以產品系統類別的申報價格為準。中選企業未申報的產品系統和未中選企業的產品系統均視為非中選產品系統。如非中選產品系統中含有中選產品系統的部件,則該部件執行該企業的中選價。
按照質量、功能與價格相匹配的原則,在陶瓷-聚乙烯類髖關節產品系統及合金-聚乙烯類髖關節產品系統中,髖臼內襯材質為高交聯聚乙烯或高交聯聚乙烯(含抗氧化劑)的產品與超高分子量聚乙烯材質的產品按一定比例比價。
在同一產品系統類別中,綜合考慮國家組織人工關節首輪集中帶量采購中選企業履約情況,對履約良好的企業考慮優先在競價比價價格方面予以適當傾斜;對于履約不佳的企業考慮在競價比價價格等方面予以相應約束。
(四)擬中選規則
各競價單元內企業以產品系統類別開展競價,通過價格競爭產生擬中選企業。
1.規則一:A、B競價單元內,按有效申報企業競價比價價格由低到高排序,確定入圍企業。入圍企業的產品系統競價比價價格不高于最高有效申報價(具體另行公告)。最多入圍企業數量詳見下表。
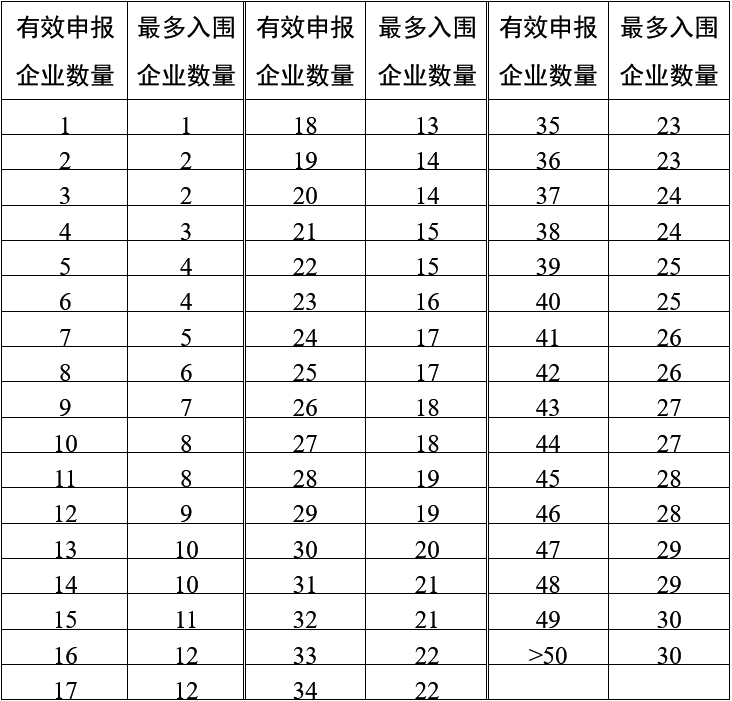
?
取得入圍資格的企業,在滿足價差控制在合理范圍等條件下(具體另行公告),獲得擬中選資格。
2.規則二:針對未按規則一獲得擬中選資格的有效申報企業,采用適當方式,在保證公平競爭、保持競爭強度、去除虛高價格空間前提下,基于首輪集采中選價并適當考慮首輪集采時不同產品系統類別競爭強度差異,促進更多價格低于一定水平的企業中選,增強預期穩定性,不受擬中選規則一中入圍企業數量的限制。
(五)分量規則
堅持臨床需求導向,尊重醫療機構自主選擇,按照量價掛鉤原則,實行梯度帶量,引導競爭。
第一步,分基礎量。中選企業按照競價比價價格由低到高排名,根據排名先后梯度分配基礎量,排名靠前的中選企業帶量比例較高,排名靠后的中選企業帶量比例較低。
第二步,分剩余量。中選產品系統未分配的意向采購量及非中選產品系統的意向采購量共同組成剩余量,由醫療機構按一定規則自主選擇,將剩余量分配給中選企業,對中選順位靠前的企業予以傾斜,對中選順位靠后的企業適當約束。剩余量可在同產品系統類別跨A、B競價單元分配。剩余量分配時,適當考慮用量較少醫療機構的特殊性。
(六)采購周期
本次接續采購周期3年,以聯盟各地區中選結果實際執行日起計算。采購周期內醫療機構每年應完成當年協議采購量,超出協議采購量的部分,中選企業仍需按中選價格供應,直至采購周期屆滿。
(七)產品新增
采購周期內,如中選企業未申報或新獲批的產品系統接受該企業同產品系統類別中選價,由企業向聯合采購辦公室申請,可作為中選產品系統掛網;如未中選企業或新獲批企業的產品系統接受同產品系統類別最高中選價,由企業向聯合采購辦公室申請后掛網,不作為非中選產品系統統計,并允許其在下一年度采購協議期按中選產品系統掛網;如中選產品注冊證更新,中選資格及中選價格維持不變。
(八)其他要求
1.采購周期內,醫療機構優先使用中選產品系統,并確保完成協議采購量。
2.各省(區、市)進一步加強對非中選產品系統的掛網管理,要按照性能和價格相匹配的原則,考慮與中選產品系統的合理比價關系,將非中選產品掛網價格進一步導入合理區間,并加強執行過程中的監測監管。
五、申報企業信息維護
申報企業使用數字證書登錄國家醫保服務平臺-國家組織高值醫用耗材集中采購信息填報系統(fuwu.nhsa.gov.cn),進入人工關節集采系統,在“供應區域”菜單,填報供應中國市場的年最大產能信息,確定本企業人工關節產品在聯盟地區的供應區域范圍,具體到地市級地區;在“企業間關系”菜單,填報企業間關聯關系(含同一實際控制人、存在控股關系、多家企業委托一家企業申報等)。具體操作方法詳見系統內操作手冊。
六、聯系方式
聯系電話:022-24538159;聯系傳真:022-24538991。
服務時間:9:00-12:00,14:00-16:30,節假日除外。
聯系地址:天津陳塘科技商務區服務中心四樓(天津市河西區洞庭路20號)
其他未盡事宜另行公告。
國家組織高值醫用耗材聯合采購辦公室
2024年2月23日